北京时间3月24日早4:30,美国食品药品管理局(FDA)公告称,批准认证美国吉利德科学公司的瑞德西韦(Remdesivir)孤儿药认证,适应症为新型冠状病毒肺炎(COVID-19)。 瑞德西韦是美国吉利德公司正在研发中的一种试验性的抗病毒药物,未获批上市,先前曾用于抗埃博拉病毒感染的临床试验,且在体外及动物研究中对严重急性呼吸综合征(SARS)冠状病毒和中东呼吸综合征(MERS)冠状病毒等显示较好的抗病毒活性。
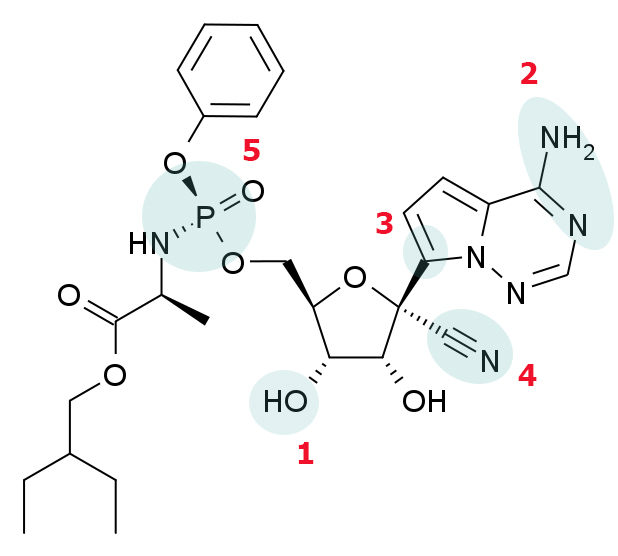
新冠肺炎暴发以来,瑞德西韦被视为最具潜力的在研药物。此前世界卫生组织在中国考察疫情后表示,瑞德西韦可能是治疗新冠肺炎唯一有效的药物。今年1月,基于“同情用药”原则,美国研究人员对一名新冠病毒感染者使用了瑞德西韦,患者症状在一两天内显著改善,使这种药物备受瞩目。
孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物上市后针对所批准适应症为期7年的市场独占期。
最重要的是,美国为孤儿药新药申请提供了快速审批通道,孤儿药在临床试验申报中可享受各种加快审评的政策。这意味着获得孤儿药认证之后,瑞德西韦注册上市的进程将大大加快。
2月26日,吉利德科学公司(Nasdaq: GILD)在官网宣布,启动两项三期临床研究,以评估瑞德西韦在治疗感染新型冠状病毒成人病例中的安全性和有效性。
从今年3月开始,这些随机、开放、多中心的研究将在主要分布在亚洲国家,以及全球其他确诊病例较多的国家的医疗机构展开,入组约1000名患者。该研究将评估两种静脉注射给药时间下的瑞德西韦的效果。两项研究的主要终点是临床改善。